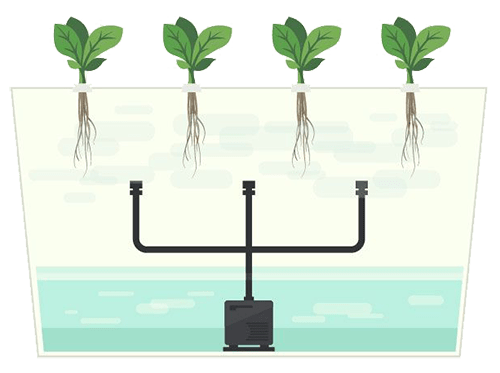
La capacità di lasciare e mescolare i nutrienti è fondamentale per padroneggiare l’idroponica. Ma dovrebbe essere chiaro che questo è un processo molto laborioso e che richiede tempo. Anche gli idroponici esperti preferiscono sistemi di alimentazione già pronti come il kit di coltura idroponica. Questa sarà un’opzione più adatta per un principiante e ti eviterà di immagazzinare un’abbondanza di materie prime e attrezzature di laboratorio.
Successivamente, considereremo un esempio di composizione e preparazione di una soluzione di una data concentrazione di nutrienti.
Prima di iniziare a formulare la miscela di nutrienti, è necessario selezionare la soluzione più adatta alla coltura, al clima e al metodo di coltivazione. Le raccomandazioni per l’alimentazione delle miscele di nutrienti sono descritte nell’articolo “Selezione di soluzioni nutritive” e la base delle soluzioni per la selezione è descritta nella sezione del sito Web “Ricette di miscele di nutrienti per l’idroponica”.
Per un esempio di calcolo, prendiamo la famosissima “Soluzione nutritiva di Chesnokov e Bazyrina”. La concentrazione dei nutrienti è espressa in milligrammi di un elemento in 1 litro di soluzione [mg/l]. Sul sito web appare così:
Per comodità, consiglio di compilare una tabella, è conveniente utilizzare Microsoft Excel o programmi specializzati per il calcolo delle miscele di nutrienti. La tabella sarà simile a questa:
Componente di fusione
Facciamo, g / l
N
P
K
Ca
Mg
…
Nella soluzione finita, mg / l
Soluzione specificata, mg/l
Trasferiamo la concentrazione degli elementi dalla base alla tabella (non prendiamo in considerazione il contenuto di ammonio e azoto nitrico in questo esempio).
Componente di fusione
Facciamo, g / l
N
P
K
Ca
Mg
…
Nella soluzione finita, mg / l
Soluzione specificata, mg/l
140
38.5
190
165
30
Successivamente, è necessario selezionare le sostanze da cui verrà preparata la miscela futura. Di norma, questi sono fertilizzanti minerali.
Vale la pena partire da un componente, che vogliamo aggiungere con una sola sostanza. Preferisco iniziare con calcio o magnesio. Cominciamo dal magnesio.
magnesio

È noto che per 1 unità di massa di MgO, ci sono 0,603 unità di massa di Mg. Questa cifra è calcolata in base alle masse molari di composti e sostanze semplici e può essere trovata sotto il termine “fattore di ossido”. Queste cifre per diverse sostanze sono fornite nell’articolo “Fattore di ossido” o possono essere calcolate dal calcolatore online delle masse molari nella pagina dell’articolo “Massa molare dei composti chimici”.
Facciamo una semplice proporzione:
- Prendiamo 16,2 g di MgO come 1 unità di massa,
- allora x g Mg è 0,603 unità di massa.
x = 16.2 · 0.603 = 9.77 g
Otteniamo il seguente risultato: 100 grammi di fertilizzante contengono 9,77 grammi di magnesio puro. Inseriamo i dati nella tabella:
Componente di fusione
Facciamo, g / l
N
P
K
Ca
Mg
MgO
solfato di magnesio, peso%
9.77
16.2
…
Nella soluzione finita, mg / l
Soluzione specificata, mg/l
140
38.5
190
165
30
Ora devi calcolare la quantità di fertilizzante che deve essere applicata per ottenere una soluzione con una concentrazione di magnesio di 30 mg / l. Una concentrazione di 30 mg/L ci dice che 1 litro di soluzione contiene 30 milligrammi di magnesio, ovvero, tradotti in grammi, 0,03 grammi di magnesio. Per il calcolo, componiamo ancora una semplice proporzione:
- 100 grammi di fertilizzante applicano 9,77 grammi di Mg,
- quindi x grammo di fertilizzante aggiungerà 0,03 grammi di Mg.
x = 100 · 0.03 / 9.77 = 0.31
Conclusione: è necessario applicare 0,31 grammi di fertilizzante al solfato di magnesio per 1 litro di soluzione. Compiliamo la tabella:
Componente di fusione
Facciamo, g / l
N
P
K
Ca
Mg
MgO
solfato di magnesio, peso%
0,31
9.77
16.2
…
Nella soluzione finita, mg / l
30
Soluzione specificata, mg/l
140
38.5
190
165
30
calcio

Il fattore di ossido per CaO è 0,715. Fertilizzante puro contenuto di calcio:
Ca = 27 · 0.715 = 19.3%
È necessario aggiungere alla soluzione 165 mg di calcio per 1 litro.
- 100 grammi di fertilizzante introducono 19,3 grammi di Ca,
- quindi x grammo di fertilizzante aggiungerà 0,165 grammi di Ca.
x = 100 · 0.165 / 19.3 = 0.855
Conclusione: è necessario applicare 0,855 grammi di fertilizzante a base di nitrato di calcio per 1 litro di soluzione.
Importante! Vale la pena considerare che il nitrato di calcio, oltre al calcio, introduce anche azoto nella soluzione. Il contenuto di azoto nel fertilizzante è del 14,9%. Si scopre che 0,855 grammi di fertilizzante oltre al calcio aggiungeranno 0,127 grammi di azoto (0,855 14,9 / 100), che è pari a 127 mg. Compiliamo la tabella:
Componente di fusione
Facciamo, g / l
N
P
K
Ca
CaO
Mg
MgO
solfato di magnesio, peso%
0,31
9.77
16.2
Nitrato di calcio, peso%
0,855
14,9
19,3
27
…
Nella soluzione finita, mg / l
127
165
30
Soluzione specificata, mg/l
140
38.5
190
165
30
fosforo
Il fosforo viene spesso aggiunto alla soluzione nutritiva sotto forma di superfosfati o monofosfato di potassio. Nell’esempio, useremo il monofosfato di potassio. La composizione del fertilizzante sarà la seguente: P2O5 = 50%, K2O = 33%. Poiché il fertilizzante applica sia il potassio che il fosforo, vale la pena fare una scelta su cosa calcolare. Ad esempio, considera lo scenario peggiore, quando non indoviniamo bene la prima volta. Inoltre, sarà più chiaro di cosa si tratta.
Iniziamo il calcolo per il potassio. Simile ai calcoli precedenti:
Fattore di ossido per K2O è 0.83. Fertilizzante puro contenuto di potassio:
È necessario aggiungere alla soluzione 190 mg di potassio per 1 litro.
- 100 grammi di fertilizzante applicano 27,39 grammi di K,
- quindi x grammo di fertilizzante aggiungerà 0,190 grammi K.
x = 100 · 0.190 / 27.39 = 0.69
Conclusione: è necessario produrre 0,69 grammi di fertilizzante “monofosfato di potassio” per 1 litro di soluzione.
Importante! Insieme al potassio viene introdotto anche il fosforo.
Fattore di ossido per P2O5 è 0.436. Fertilizzante contenuto di fosforo puro:
P = 50 · 0.436 = 21.8 %
Aggiungiamo alla soluzione 0,69 grammi di fertilizzante “monofosfato di potassio” e quindi 0,15 grammi di fosforo (0,69 · 21,8 / 100). 0,15 grammi = 150 mg, che è significativamente più del necessario. Conclusione: stiamo calcolando partendo dal fosforo.
Calcolo per il fosforo. Simile ai calcoli precedenti:
Fattore di ossido per P2O5 è 0.436. Fertilizzante contenuto di fosforo puro:
P = 50 · 0.436 = 21.8 %
È necessario aggiungere alla soluzione 38,5 mg di fosforo per 1 litro.
- 100 grammi di fertilizzante applicano 21,8 grammi di P,
- quindi x grammo di fertilizzante aggiungerà 0,0385 grammi P.
x = 100 · 0.0385 / 21.8 = 0.177
Conclusione: è necessario produrre 0.177 grammi di fertilizzante “monofosfato di potassio” per 1 litro di soluzione.
Importante! Insieme al fosforo viene aggiunto anche il potassio.
Fattore di ossido per K2O è 0.83. Fertilizzante puro contenuto di potassio:
K = 33 · 0.83 = 27.39%
Aggiungiamo alla soluzione 0.177 grammi di fertilizzante “monofosfato di potassio” e quindi 0,048 grammi di potassio (0.177 · 27.39 / 100). Compiliamo la tabella:
Componente di fusione
Facciamo, g / l
N
P
P2O5
K
K2O
Ca
CaO
Mg
MgO
solfato di magnesio, peso%
0,31
9.77
16.2
Nitrato di calcio, peso%
0,855
14,9
19,3
27
Monofosfato di potassio, % in peso
0.177
21.8
50
27.39
33
…
Nella soluzione finita, mg / l
127
38.5
48
165
30
Soluzione specificata, mg/l
140
38.5
190
165
30
azoto
Resta da aggiungere un po ‘di azoto e potassio alla soluzione. Cominciamo con l’azoto. L’azoto viene aggiunto alla soluzione nutritiva in varie forme. Useremo il nitrato di potassio, poiché è più appropriato data la mancanza di potassio. Diciamo che il nitrato di potassio (nitrato di potassio) ha la seguente composizione: N = 13.6%, K2O = 46%.
Il contenuto di azoto nel fertilizzante è del 13.6%. È necessario aggiungere 13 mg di azoto (140-127 mg). Facciamo la proporzione:
- 100 grammi di fertilizzante applicano 13,6 grammi di N,
- foglie x grammo di fertilizzante Si applica 0,013 grammi di N.
x = 100 · 0.013 / 13.6 = 0.096
Conclusione: è necessario applicare 0.096 grammi di fertilizzante a base di nitrato di potassio per 1 litro di soluzione.
Importante! Il potassio viene aggiunto insieme all’azoto.
Fattore di ossido per K2O è 0.83. Fertilizzante puro contenuto di potassio:
K = 46 · 0.83 = 38,18%
Aggiungiamo alla soluzione 0.096 grammi di fertilizzante a base di nitrato di potassio e quindi 0,037 grammi di potassio (0.096 · 38,18 / 100). In totale, 85 mg di potassio (37 + 48 g) in soluzione. Compiliamo la tabella:
Componente di fusione
Facciamo, g / l
N
P
P2O5
K
K2O
Ca
CaO
Mg
MgO
solfato di magnesio, peso%
0,31
9.77
16.2
Nitrato di calcio, peso%
0,855
14,9
19,3
27
Monofosfato di potassio, % in peso
0.177
21.8
50
27.39
33
Nitrato di potassio, % in peso
0,096
13,6
38,18
46
…
Nella soluzione finita, mg / l
140
38.5
85
165
30
Soluzione specificata, mg/l
140
38.5
190
165
30
potassio
Completiamo la preparazione della soluzione aggiungendo la quantità mancante di potassio. Per l’introduzione del potassio, e la non introduzione di altri elementi, applichiamo il fertilizzante “solfato di potassio”. Diciamo che il solfato di potassio contiene: K2O = 50%.
Fattore di ossido per K2O è 0.83. Fertilizzante puro contenuto di potassio:
K = 50 · 0.83 = 41.5%
È necessario aggiungere alla soluzione 105 mg di potassio per 1 litro (190-85 g).
- 100 grammi di fertilizzante applicano 41,5 grammi di K,
- quindi x grammo di fertilizzante aggiungerà 0,105 grammi K.
x = 100 · 0.105 / 41,5 = 0.253
Conclusione: è necessario applicare 0,253 grammi di fertilizzante al solfato di potassio per 1 litro di soluzione. Compiliamo la tabella:
Componente di fusione
Facciamo, g / l
N
P
P2O5
K
K2O
Ca
CaO
Mg
MgO
solfato di magnesio, peso%
0,31
9.77
16.2
Nitrato di calcio, peso%
0,855
14,9
19,3
27
Monofosfato di potassio, % in peso
0.177
21.8
50
27.39
33
Nitrato di potassio, % in peso
0,096
13,6
38,18
46
Solfato di potassio, % in peso
0,253
41,5
50
Nella soluzione finita, mg / l
140
38.5
190
165
30
Soluzione specificata, mg/l
140
38.5
190
165
30
La soluzione pronta corrisponde a quella già pronta: la soluzione è composta correttamente. Per preparare una maggiore quantità di soluzione, effettuiamo un semplice ricalcolo moltiplicando le quantità applicate per il volume richiesto in litri. Esempio di calcolo per 5 litri:
Componente di fusione
Facciamo, g / l
Facciamo, g / 5l
Solfato di magnesio
0,31
1,55
Nitrato di calcio
0,855
4,275
Monofosfato di potassio
0.177
0,885
Nitrato di potassio
0,096
0,48
Solfato di potassio
0,253
1,265
Come sai, l’acqua per la preparazione delle soluzioni nutritive può contenere una certa quantità di sali disciolti, che dovrebbe essere presa in considerazione durante la compilazione delle soluzioni nutritive. Diciamo che l’acqua ha la seguente composizione:
Nome Ca Mg K Contenuto, mg / l 50 25 30
Tutto ciò che occorre fare è correggere la composizione della soluzione prima di iniziare il calcolo. Sembra così:
Componente di fusione
Facciamo, g / l
N
P
K
Ca
Mg
…
Nella soluzione finita, mg / l
Soluzione specificata tenendo conto della composizione dell’acqua, mg / l
140
38,5
160
115
5
Soluzione specificata, mg/l
140
38.5
190
165
30
Acqua, mg/l
30
50
25
Successivamente, eseguiamo il calcolo, in modo simile alle istruzioni pubblicate sopra.
Pesare quantità piccole e minime di sostanze può essere difficile se non è disponibile una bilancia analitica. Utilizzando bilance domestiche per questo scopo, non si può mai essere sicuri della precisione di pesatura di almeno 0,5 g Esiste un modo semplice per preparare soluzioni senza avere bilance precise. Consideriamo l’esempio di una soluzione di oligoelementi secondo Hoagland.
Prepariamo in acqua distillata una soluzione allo 0,5% di tutti i composti di oligoelementi di cui abbiamo bisogno solo in piccole quantità (ad esempio cloruro di stagno, ioduro di potassio, nitrato di cobalto, ecc.). Quindi, scioglieremo, ad esempio, 5 g di ioduro di potassio in 1 litro di acqua distillata. Se abbiamo bisogno solo di 0,5 g, prendiamo semplicemente 100 metri cubi da questa soluzione. cm, che contengono esattamente 0,5 g La quantità richiesta di centimetri cubi viene misurata con una pipetta, una siringa o un becher accurati, anche se economici. Usando questo metodo, non bisogna dimenticare che, secondo la ricetta per la preparazione della soluzione di Hoagland, tutte le quantità sono indicate per 18 litri di acqua. Pertanto, dopo aver sciolto tutti i concentrati da noi preparati separatamente in circa 10 litri di acqua, solo allora portiamo la quantità totale di liquido a 18 litri con acqua.
Acidificazione della soluzione nutritiva
La soluzione nutritiva di solito deve essere acidificata. L’assorbimento di ioni da parte delle piante provoca una graduale alcalinizzazione della soluzione. Qualsiasi soluzione con un pH di 7 o più spesso dovrà essere regolata al pH ottimale. Vari acidi possono essere usati per acidificare la soluzione nutritiva, ma di solito si usa l’acido solforico perché è sempre disponibile ed economico.
Quando si regola il pH sia con acidi che con alcali, è necessario indossare guanti di gomma per evitare ustioni alla pelle. Un chimico esperto è abile nel maneggiare l’acido solforico concentrato, aggiungendo l’acido goccia a goccia all’acqua. Ma per gli idroponisti alle prime armi, forse è meglio rivolgersi a un chimico esperto e chiedergli di preparare una soluzione di acido solforico al 25%. Mentre si aggiunge l’acido, si agita la soluzione e se ne determina il pH. Avendo appreso la quantità approssimativa di acido solforico, in futuro può essere aggiunto da un cilindro graduato.
L’acido solforico va aggiunto in piccole porzioni per non acidificare troppo la soluzione, che poi dovrà essere nuovamente alcalinizzata. In un lavoratore inesperto, l’acidificazione e l’alcalinizzazione possono continuare all’infinito. Oltre a far perdere tempo e reagenti, tale regolazione sbilancia la soluzione nutritiva a causa dell’accumulo di ioni non necessari alle piante.
Alcalinizzazione della soluzione nutritiva
Le soluzioni troppo acide sono rese alcaline con sodio caustico (idrossido di sodio). Come suggerisce il nome, è corrosivo, quindi è necessario indossare guanti di gomma. Si consiglia di acquistare idrossido di sodio in forma di pillola. Nei negozi di prodotti chimici domestici, l’idrossido di sodio può essere acquistato come scovolino, come Mole. Sciogliere un pellet in 0,5 L di acqua e aggiungere gradualmente la soluzione alcalina alla soluzione nutritiva con costante agitazione, controllandone frequentemente il pH. Nessun calcolo matematico può calcolare la quantità di acido o alcali da aggiungere in un dato caso.
Se si desidera coltivare più colture nello stesso pallet, è necessario selezionarle in modo che coincidano non solo il loro pH ottimale, ma anche le esigenze di altri fattori di crescita. Ad esempio, i narcisi gialli e i crisantemi necessitano di un pH di 6,8, ma di condizioni di umidità diverse, quindi non possono essere coltivati sullo stesso pallet. Se dai ai narcisi tanta umidità quanto i crisantemi, i bulbi del narciso marciranno. Negli esperimenti, il rabarbaro ha raggiunto il suo massimo sviluppo a pH 6,5, ma potrebbe crescere anche a pH 3,5. L’avena, che preferisce un pH di circa 6, produce buoni raccolti a pH 4, se la dose di azoto nella soluzione nutritiva viene notevolmente aumentata. Le patate crescono in un intervallo di pH abbastanza ampio, ma prosperano meglio a un pH di 5,5. Al di sotto di questo pH si ottengono anche rese elevate di tuberi, ma acquistano un sapore aspro. Per ottenere le massime rese di alta qualità, il pH delle soluzioni nutritive deve essere regolato con precisione.