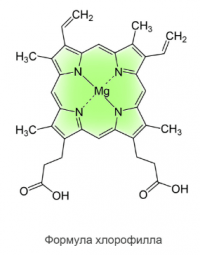
Veden kovuus on yhdistelmä kemiallisia ja fysikaalisia ominaisuuksia, jotka liittyvät maa-alkalimetallien liuenneiden suolojen, pääasiassa kalsiumin ja magnesiumin, ns. ”kovuussuolojen” pitoisuuteen.
Vesi, joka sisältää 100-150 mg kalsiumia litrassa, on hyväksyttävää hydroponiseen käyttöön, ja periaatteessa useimmille kasveille ei ole tarpeen lisätä kalsiumia.
Pehmeä vesi sisältää alle 50 mg kalsiumia litrassa. Onnistuneen kasvien kasvun varmistamiseksi on tarpeen lisätä lisäksi kalsium- ja magnesiumsuoloja.
Hydroponisten lannoitteiden valmistajat ottavat huomioon kalsiumin ja magnesiumin koostumuksensa ja valmistavat muunnelmia lannoitteista sekä kovalle että pehmeälle vedelle.
Veden kovuus erotetaan väliaikaiseen (karbonaatti) ja pysyvään.
Väliaikainen veden kovuus
Väliaikainen kovuus on eräänlainen veden kovuus, joka johtuu liuenneen kalsiumkarbonaatin ja magnesiumkarbonaatin läsnäolosta. Kun nämä mineraalit liukenevat liuokseen, kalsium- ja magnesiumkationit (Ca2+, Mg2+) ja karbonaatti- ja bikarbonaattianionit32-HCO3,). Hydroponiikan optimaalinen pH on 5,5. Veden pH on liian korkea, jos kasteluvesi sisältää merkittäviä määriä karbonaattia ja bikarbonaattia (CO32-HCO3,). Näin on yleensä kaivovettä käytettäessä. Siksi tämä vesi on käsiteltävä hapolla HCO:n neutraloimiseksi.3, ja alentaa ravinneliuoksen pH:ta. Lisättävän hapon määrä määräytyy HCO-pitoisuuden mukaan3,… Kun veteen lisätään happoa, hapon protoni neutraloi bikarbonaatin ja liuoksen pH laskee. Kalsium (tai magnesium) pysyy kasvien käytettävissä, ja happoanioni pysyy liuenneena veteen. Esimerkiksi typpihapon lisääminen aiheuttaa seuraavan reaktion:
Ca2+ + 2HCO3, + 2HNO3 ⇋ Ca2+ + 2CO2 + 2H2O + 2NO3,
Typpihappoa käytetään laajalti tähän tarkoitukseen, mutta myös fosforihappoa ja sen johdannaisia, kuten ureafosfaattia, voidaan käyttää. Lisäämällä happoa lisäät siihen liittyvien anionien, kuten nitraatin ja fosfaatin, pitoisuutta liuoksessa. Nämä arvot eivät saa ylittää ravinneliuokselle vaadittavaa pitoisuutta. Tämä rajoittaa hapon määrää, joka voidaan lisätä neutraloimaan HCO.3… Näin ollen HCO:n alkuperäinen pitoisuus3, vedessä se on suuri laatuongelma.
Bikarbonaatin neutralointi hapolla käynnistää hiilidioksidin (CO2) ja vettä. CO2 on poistuttava vapaasti ravintoliuoksesta; muuten liuoksen pH ei laske ja vaihtelee. Tämä tarkoittaa, että hapon ja bikarbonaatin reaktion on tapahduttava avoimissa järjestelmissä, kuten avoimessa sekoitussäiliössä.