Väteexponent (pH-faktor) Det är ett mått på aktiviteten av vätejoner i en lösning, som kvantitativt uttrycker deras surhet. När pH-värdet inte är på optimala nivåer, börjar växter att förlora sin förmåga att absorbera några av de element som är nödvändiga för en sund tillväxt. Alla växter har en specifik pH-nivå som möjliggör maximala tillväxtresultat. De flesta växter föredrar en något sur växtmiljö (mellan 5.5 och 6.5).
Väteexponent i formler
I mycket utspädda lösningar är pH lika med koncentrationen av vätejoner. Lika i modul och motsatt tecken till decimallogaritmen för aktiviteten av vätejoner, uttryckt i mol per liter:
pH = -lg [H+]
Under standardförhållanden ligger pH-värdet i intervallet 0 till 14. I rent vatten, vid neutralt pH, är koncentrationen H+ är lika med OH-koncentrationen, och det är 1-7 mol per liter. Det högsta möjliga pH-värdet definieras som summan av pH och pOH och är lika med 14.
I motsats till vad många tror kan pH-värdet variera inte bara i intervallet 0 till 14, utan kan också gå över dessa gränser. Till exempel, vid en vätejonkoncentration [H+] = 10-15 mol/l, pH = 15, vid en koncentration av hydroxidjoner [OH,] 10 mol/L pOH = -1.
Det är viktigt att förstå! pH-skalan är logaritmisk, vilket innebär att varje förändringsenhet motsvarar en tiofaldig förändring av koncentrationen av vätejoner. En lösning med pH 6 är med andra ord tio gånger surare än en lösning med pH 7, och en lösning med pH 5 kommer att vara tio gånger surare än en lösning med pH 6 och hundra gånger surare än en lösning med pH 7. Det betyder att när du justerar pH i din näringslösning och du behöver ändra pH i två punkter (till exempel från 7.5 till 5.5) bör du använda tio gånger mer pH-korrigerare än om du skulle ändra pH på bara en punkt (från 7.5 till 6.5).
Metoder för att bestämma pH-värdet.
Olika metoder används i stor utsträckning för att bestämma pH-värdet för lösningar. PH kan uppskattas grovt med indikatorer, noggrant mätas med en pH-mätare eller analytiskt bestämmas genom syra-bastitrering.
Syra-basindikatorer
För en grov uppskattning av koncentrationen av vätejoner används syra-basindikatorer i stor utsträckning – organiska färgämnen, vars färg beror på mediets pH. De mest kända indikatorerna inkluderar lackmus, fenolftalein, metylorange (metylorange) och andra. Indikatorer kan finnas i två olika färgformer: sura eller basiska. Färgförändringen för varje indikator sker i dess surhetsgrad, vanligtvis 1-2 enheter.
universell indikator

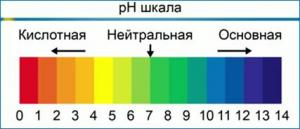
Lösningar av sådana blandningar: ”universella indikatorer” är vanligtvis impregnerade med remsor av ”indikatorpapper”, med hjälp av vilka det är möjligt att snabbt bestämma (med en noggrannhet av pH-enheter, eller till och med tiondelar av ett pH) surheten hos undersökte vattenlösningar. För en mer exakt bestämning jämförs färgen på indikatorpapperet som erhålls genom att applicera en droppe lösning omedelbart med en referensfärgskala, vars form visas i bilderna.
Bestämning av pH med indikatormetoden är svår för grumliga eller färgade lösningar.
Med tanke på att de optimala pH-värdena för näringslösningar inom hydrokultur har ett mycket smalt intervall (vanligtvis 5.5 till 6.5), använder jag också andra kombinationer av indikatorer. Till exempel har vårt flytande pH-test ett arbetsområde och skala från 4.0 till 8.0, vilket gör det mer exakt än ett universellt indikatorpapper.
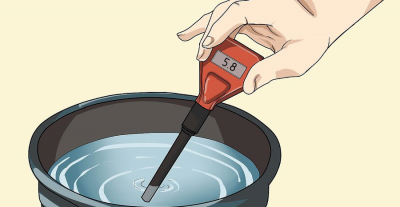
PH-mätare

För en mer detaljerad studie av ämnet rekommenderar vi att du besöker motsvarande sektion av forumet: ”pHmeters”.
Volumetrisk analysmetod
Den analytiska volumetriska metoden, syra-bastitrering, ger också exakta resultat för att bestämma surheten i lösningar. En lösning med känd koncentration (titrant) tillsätts droppvis till testlösningen. När de blandas uppstår en kemisk reaktion. Ekvivalenspunkten, den tid då titranten är exakt tillräcklig för att fullständigt fullborda reaktionen, ställs in av en indikator. Dessutom, med kännedom om koncentrationen och volymen av den tillsatta titreringslösningen, beräknas lösningens surhet.
Temperaturens inverkan på pH-värdena

Justera näringslösningens pH
Försurning av näringslösningen.
I allmänhet är det nödvändigt att surgöra näringslösningen. Absorptionen av joner av växter orsakar en gradvis alkalisering av lösningen. Varje lösning som har ett pH på 7 eller mer måste ofta justeras till det optimala pH. Olika syror kan användas för att surgöra näringslösningen. Svavelsyra eller fosforsyror är de mest använda. En bättre lösning för hydroponiska lösningar är buffertar som pH minus Bloom och pH minus Grow. Dessa medel ger inte bara pH-värdena till det optimala, utan stabiliserar också värdena under en längre period.
Vid justering av pH med syror och alkalier bör gummihandskar användas för att undvika brännskador på huden. En erfaren kemist är skicklig på att hantera koncentrerad svavelsyra och tillsätta syran droppvis i vattnet. Men för nybörjare kan det vara bäst att vända sig till en erfaren kemist och be honom att förbereda en 25 % svavelsyralösning. Medan syran tillsätts omrörs lösningen och dess pH bestäms. Efter att ha lärt sig den ungefärliga mängden svavelsyra, kan den i framtiden läggas till från en graderad cylinder.
Svavelsyra bör tillsättas i små portioner för att inte översyra lösningen, som sedan måste göras alkalisk igen. Hos en oerfaren arbetare kan försurning och alkalisering fortsätta i det oändliga. Förutom att slösa tid och reagens, obalanserar sådan reglering näringslösningen på grund av ackumuleringen av onödiga joner för växterna.
Alkalisering av näringslösningen.
Alltför sura lösningar görs alkaliska med kaustikt natrium (natriumhydroxid). Som namnet antyder är det frätande, så gummihandskar bör användas. Det rekommenderas att köpa natriumhydroxid i pillerform. Natriumhydroxid kan köpas som piprensare i hushållskemikalier, som Mole. Lös upp ett granulat i 0,5 L vatten och tillsätt gradvis den alkaliska lösningen till näringslösningen under konstant omrörning, kontrollera ofta dess pH. Ingen matematisk beräkning kan beräkna mängden syra eller alkali som ska tillsättas i ett givet fall.
Om du vill odla flera grödor på en murslev måste du välja dem så att de matchar inte bara deras optimala pH-värde, utan även behoven hos andra tillväxtfaktorer. Till exempel behöver påskliljor och gula krysantemum ett pH på 6,8, men olika luftfuktighetsförhållanden, så de kan inte odlas på samma pall. Om du ger påskliljor lika mycket fukt som krysantemum kommer påskliljorna att ruttna. I experiment nådde rabarber sin maximala utveckling vid pH 6,5, men kunde växa även vid pH 3,5. Havre, som föredrar ett pH på cirka 6, ger goda skördar vid pH 4, om dosen av kväve i näringslösningen ökar avsevärt. Potatis växer i ett ganska brett pH-område, men den trivs bäst vid ett pH på 5,5. Under detta pH erhålls också höga skördar av knölar, men de får en bitter smak. För att få maximal avkastning av hög kvalitet måste näringslösningarnas pH justeras exakt.