Vodíkový exponent (faktor pH) Je to míra aktivity vodíkových iontů v roztoku, kvantitativně vyjadřuje jejich kyselost. Když pH není na optimální úrovni, rostliny začnou ztrácet schopnost absorbovat některé prvky nezbytné pro zdravý růst. Všechny rostliny mají specifickou úroveň pH, která umožňuje maximální výsledky růstu. Většina rostlin preferuje mírně kyselé pěstební prostředí (mezi 5.5 a 6.5).
Vodíkový exponent ve vzorcích
Ve velmi zředěných roztocích se pH rovná koncentraci vodíkových iontů. Rovná se v modulu a opačném znaménku k dekadickému logaritmu aktivity vodíkových iontů, vyjádřeno v molech na litr:
pH = -lg [H+]
Za standardních podmínek je hodnota pH v rozmezí 0 až 14. V čisté vodě je při neutrálním pH koncentrace H+ rovná se koncentraci OH, a je 1-7 mol na litr. Maximální možná hodnota pH je definována jako součet pH a pOH a je rovna 14.
Na rozdíl od všeobecného přesvědčení se pH může měnit nejen v rozmezí 0 až 14, ale může jít i za tyto limity. Například při koncentraci vodíkových iontů [H+] = 10-15 mol / l, pH = 15, při koncentraci hydroxidových iontů [OH,] 10 mol/l pOH = -1.
Je důležité pochopit! Stupnice pH je logaritmická, což znamená, že každá jednotka změny se rovná desetinásobné změně koncentrace vodíkových iontů. Jinými slovy, roztok s pH 6 je desetkrát kyselejší než roztok s pH 7 a roztok s pH 5 bude desetkrát kyselejší než roztok s pH 6 a stokrát kyselejší než roztok s pH 7. Znamená to, že když upravujete pH svého živného roztoku a potřebujete změnit pH ve dvou bodech (například ze 7.5 na 5.5), měli byste použít desetkrát více pH korektoru, než kdybyste změnili pH pouze v jednom bodě (od 7.5 až 6.5).
Metody stanovení hodnoty pH.
Pro stanovení hodnoty pH roztoků se široce používají různé metody. PH lze zhruba odhadnout pomocí indikátorů, přesně změřit pH metrem nebo analyticky stanovit acidobazickou titrací.
Acidobazické indikátory
Pro hrubý odhad koncentrace vodíkových iontů se hojně používají acidobazické indikátory – organické barvící látky, jejichž barva závisí na pH média. Mezi nejznámější indikátory patří lakmus, fenolftalein, methyloranž (methyloranž) a další. Indikátory mohou existovat ve dvou různých barevných formách: kyselé nebo zásadité. Změna barvy každého indikátoru nastává v jeho rozsahu kyselosti, obvykle 1-2 jednotky.
univerzální indikátor

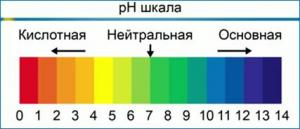
Roztoky takových směsí: „univerzální indikátory“ jsou obvykle napuštěny proužky „indikačního papírku“, pomocí kterého lze rychle (s přesností jednotek pH, případně i desetin pH) určit kyselost zkoumané vodné roztoky. Pro přesnější určení je barva indikátorového papírku získaná nanesením kapky roztoku ihned porovnána s referenční barevnou škálou, jejíž tvar je znázorněn na snímcích.
Stanovení pH indikátorovou metodou je obtížné u zakalených nebo barevných roztoků.
Vzhledem k tomu, že optimální hodnoty pH pro živné roztoky v hydroponii mají velmi úzký rozsah (obecně 5.5 až 6.5), používám i jiné kombinace indikátorů. Například náš test pH kapaliny má provozní rozsah a stupnici od 4.0 do 8.0, díky čemuž je přesnější než univerzální indikátorový papírek.
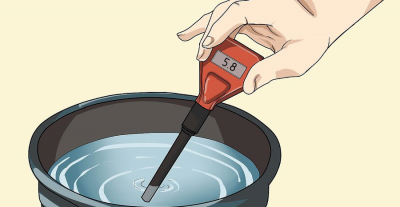
PH metr

Pro podrobnější studium předmětu doporučujeme navštívit odpovídající sekci fóra: „pHmetry“.
Objemová analytická metoda
Přesné výsledky pro stanovení kyselosti roztoků poskytuje také analytická volumetrická metoda, acidobazická titrace. Ke zkoušenému roztoku se po kapkách přidá roztok o známé koncentraci (titrační činidlo). Když se smíchají, dojde k chemické reakci. Bod ekvivalence, čas, kdy titrační činidlo přesně stačí k úplnému dokončení reakce, je nastaven indikátorem. Kromě toho se při znalosti koncentrace a objemu přidaného titračního roztoku vypočítá kyselost roztoku.
Vliv teploty na hodnoty pH

Upravte pH živného roztoku
Okyselení živného roztoku.
Obecně je nutné okyselit živný roztok. Absorpce iontů rostlinami způsobuje postupnou alkalizaci roztoku. Jakýkoli roztok, který má pH 7 nebo více, bude často nutné upravit na optimální pH. K okyselení živného roztoku lze použít různé kyseliny. Nejpoužívanější jsou kyseliny sírové nebo fosforečné. Lepším řešením pro hydroponické roztoky jsou pufry jako pH minus Bloom a pH minus Grow. Tyto prostředky nejen přivádějí hodnoty pH na optimum, ale také dlouhodobě stabilizují hodnoty.
Při úpravě pH pomocí kyselin a zásad je třeba používat gumové rukavice, aby nedošlo k popálení kůže. Zkušený chemik je zběhlý v zacházení s koncentrovanou kyselinou sírovou a přidává kyselinu po kapkách do vody. Pro začátečníky v hydroponii by ale mohlo být nejlepší obrátit se na zkušeného chemika a požádat ho o přípravu 25% roztoku kyseliny sírové. Během přidávání kyseliny se roztok míchá a stanoví se jeho pH. Když se naučíte přibližné množství kyseliny sírové, v budoucnu ji lze přidat z odměrného válce.
Kyselina sírová by se měla přidávat po malých dávkách, aby nedošlo k překyselení roztoku, který je pak nutné znovu zalkalizovat. U nezkušeného pracovníka může acidifikace a alkalizace pokračovat donekonečna. Kromě plýtvání časem a činidly taková regulace narušuje rovnováhu živného roztoku kvůli akumulaci iontů, které jsou pro rostliny nepotřebné.
Alkalizace živného roztoku.
Příliš kyselé roztoky se zalkalizují louhem sodným (hydroxid sodný). Jak název napovídá, je žíravý, proto je třeba nosit gumové rukavice. Doporučuje se koupit hydroxid sodný ve formě pilulek. Hydroxid sodný lze zakoupit jako čistič potrubí v obchodech s chemií pro domácnost, jako je Mole. Jednu granuli rozpusťte v 0,5 l vody a za stálého míchání postupně přidávejte zásaditý roztok k živnému roztoku, často kontrolujte jeho pH. Žádný matematický výpočet nemůže vypočítat množství kyseliny nebo zásady, které je třeba v daném případě přidat.
Pokud chcete pěstovat více plodin na stěrce, musíte je vybrat tak, aby odpovídaly nejen jejich optimálnímu pH, ale také potřebám dalších růstových faktorů. Například narcisy a žluté chryzantémy potřebují pH 6,8, ale různé vlhkostní podmínky, takže je nelze pěstovat na stejné paletě. Pokud dáte narcisům tolik vláhy jako chryzantémám, cibulky narcisů zahnívají. V experimentech dosáhla rebarbora maximálního rozvoje při pH 6,5, ale byla schopna růst i při pH 3,5. Oves, který preferuje pH kolem 6, dává dobré výnosy při pH 4, pokud se výrazně zvýší dávka dusíku v živném roztoku. Brambory rostou v poměrně širokém rozmezí pH, ale nejlépe se jim daří při pH 5,5. Pod tímto pH se dosahují také vysoké výnosy hlíz, které však získávají hořkou chuť. Pro dosažení maximálně kvalitních výnosů je nutné přesně upravit pH živných roztoků.