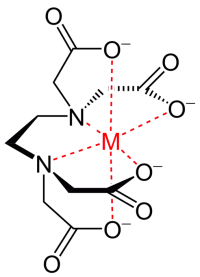
Chélates (composés chélateurs) – composés complexes chélatés formés par l’interaction d’ions métalliques avec des ligands polydentés (c’est-à-dire ayant plusieurs centres donneurs). Les chélates métalliques sont utilisés comme source d’oligo-éléments dans les mélanges nutritionnels, en raison de la forte absorption des complexes chélates par rapport aux ions métalliques libres.
Les plus populaires sont les complexes d’acide éthylènediaminetétraacétique – l’abréviation EDTA, moins souvent EDTA (l’acide A-acétate est le nom synonyme de l’acide acétique) (voir Fig.).
Tableau 1
Peignoirs en métal utilisés pour la préparation de mélanges nutritionnels
Nom du chélate Plage de stabilité, pH Ca-EDTA Ca-EDTA Ethylènediaminetétraacétate de calcium Cu-EDTA Cu-EDTA Ethylènediaminetétraacétate de cuivre 1,5-10 Fe-EDTA Fe-EDTA Ethylènediaminetétraacétate de fer 1.5-6 Fe-EDDHA Fe-EDDHA Ethylènediamine dihydroxyphénylacétate de fer 3.5 -EDDHSA 9- 4 Fe-DTPA Fe-DTPA Diéthylènetriamine pentaacétate ferreux 10-1.5 Fe-HEDTA 7-2.5 Fe-HBED 7-3.5 Mg-EDTA Mg-EDTA Magnésium éthylènediamine tétraacétate Mn-EDTA Mn-EDTA Manganèse éthylènediamine tétraacétate 12-3 Zn-EDTA Zn -EDTA Zinc éthylènediaminetétraacétate 12-2 rus. Anglais
Le type de chélates dépend du pH de la solution. Si le pH dans la zone racinaire est maintenu en dessous de 6.5, le chélate Fe-DTPA fournira une stabilité suffisante. Si le pH dépasse 6.5, l’utilisation de chélates Fe-EDDHA ou Fe-HBED est fortement recommandée.
sources
- Manuel « Solutions nutritives pour les cultures en serre » disponible, 2016