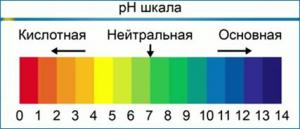
Exposant d’hydrogène (facteur pH) Est une mesure de l’activité des ions hydrogène dans une solution, exprimant quantitativement son acidité. Lorsque le pH n’est pas à des niveaux optimaux, les plantes commencent à perdre leur capacité à absorber certains des éléments nécessaires à une croissance saine. Toutes les plantes ont un niveau de pH spécifique qui permet des résultats de croissance maximum. La plupart des plantes préfèrent un milieu de croissance légèrement acide (entre 5.5 et 6.5).
Exposant d’hydrogène dans les formules
Dans des solutions très diluées, le pH est équivalent à la concentration en ions hydrogène. Égal en grandeur et opposé en signe au logarithme décimal de l’activité des ions hydrogène, exprimé en moles par litre :
pH = -lg[H+]
Dans des conditions standard, la valeur du pH est comprise entre 0 et 14. Dans l’eau pure, à pH neutre, la concentration en H+ est égal à la concentration de OH– et est 1 10-7 mole par litre. La valeur de pH maximale possible est définie comme la somme du pH et du pOH et est égale à 14.
Contrairement à la croyance populaire, le pH peut varier non seulement dans la plage de 0 à 14, mais peut également aller au-delà de ces limites. Par exemple, à une concentration d’ions hydrogène [H+] = 10-15 mol / l, pH = 15, à une concentration en ions hydroxyde [OH–] 10 mol / L pOH = -1.
Il est important de comprendre ! L’échelle de pH est logarithmique, ce qui signifie que chaque unité de changement équivaut à un changement de dix fois la concentration en ions hydrogène. Autrement dit, une solution à pH 6 est dix fois plus acide qu’une solution à pH 7, et une solution à pH 5 sera dix fois plus acide qu’une solution à pH 6 et cent fois plus acide qu’une solution à pH 7. vous ajustez le pH de votre solution nutritive et vous devez modifier le pH de deux points (par exemple, de 7.5 à 5.5), vous devez utiliser dix fois plus de correcteur de pH que si vous modifiiez le pH d’un seul point (de 7.5 à 6.5).
Méthodes de détermination du pH
Plusieurs méthodes sont largement utilisées pour déterminer la valeur du pH des solutions. Le pH peut être estimé approximativement à l’aide d’indicateurs, mesuré avec précision avec un pH-mètre ou déterminé analytiquement par titrage acide-base.
Indicateurs acido-basiques
Pour une estimation approximative de la concentration en ions hydrogène, des indicateurs acido-basiques sont largement utilisés – des substances colorantes organiques dont la couleur dépend du pH du milieu. Les indicateurs les plus connus incluent le tournesol, la phénolphtaléine, le méthyl orange (méthyl orange) et d’autres. Les indicateurs peuvent exister sous deux formes de couleurs différentes – soit acide, soit basique. Le changement de couleur de chaque indicateur se produit dans sa plage d’acidité, généralement de 1 à 2 unités.
Indicateur universel

Les solutions de tels mélanges – les « indicateurs universels » sont généralement imprégnées de bandes de « papier indicateur », à l’aide desquelles il est possible de déterminer rapidement (avec une précision d’unités de pH, voire de dixièmes de pH) l’acidité du produit étudié. solutions aqueuses. Pour une détermination plus précise, la couleur du papier indicateur obtenu lors de l’application d’une goutte de la solution est immédiatement comparée à l’échelle de couleurs de référence, dont la forme est représentée sur les images.
La détermination du pH par la méthode des indicateurs est difficile pour les solutions troubles ou colorées.
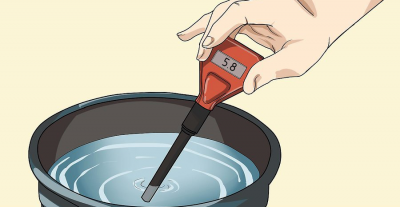
Compte tenu du fait que les valeurs de pH optimales pour les solutions nutritives en culture hydroponique ont une plage très étroite (généralement de 5.5 à 6.5), j’utilise également d’autres combinaisons d’indicateurs. Par exemple, notre test de pH liquide a une plage de fonctionnement et une échelle de 4.0 à 8.0, ce qui le rend plus précis qu’un papier indicateur universel.
pH-mètre

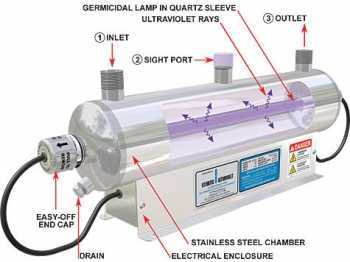
Pour une étude plus détaillée du sujet, nous vous recommandons de visiter la section correspondante du forum : « pH mètres ».
Méthode volumétrique analytique
La méthode volumétrique analytique – titrage acide-base – donne également des résultats précis pour déterminer l’acidité des solutions. Une solution de concentration connue (titrant) est ajoutée goutte à goutte à la solution d’essai. Lorsqu’ils sont mélangés, une réaction chimique se produit. Le point d’équivalence – le moment où le titrant est exactement suffisant pour terminer complètement la réaction – est fixé à l’aide d’un indicateur. De plus, connaissant la concentration et le volume de la solution titrée ajoutée, l’acidité de la solution est calculée.
Effet de la température sur les valeurs de pH

Ajustement du pH de la solution nutritive
Acidification de la solution nutritive
La solution nutritive doit généralement être acidifiée. L’absorption des ions par les plantes provoque une alcalinisation progressive de la solution. Toute solution ayant un pH de 7 ou plus devra le plus souvent être ajustée au pH optimal. Divers acides peuvent être utilisés pour acidifier la solution nutritive. Les acides sulfurique ou phosphorique sont les plus couramment utilisés. Une meilleure solution pour les solutions hydroponiques sont les tampons tels que pH moins Bloom et pH moins Grow. Ces fonds apportent non seulement les valeurs de pH à l’optimum, mais stabilisent également les valeurs pendant une longue période.
Lors de l’ajustement du pH avec des acides et des alcalis, des gants en caoutchouc doivent être portés pour éviter les brûlures de la peau. Un chimiste expérimenté est habile à manipuler l’acide sulfurique concentré, en ajoutant l’acide goutte à goutte à l’eau. Mais pour les hydroponistes novices, il vaut peut-être mieux se tourner vers un chimiste expérimenté et lui demander de préparer une solution d’acide sulfurique à 25%. Pendant que l’acide est ajouté, la solution est agitée et son pH est déterminé. Ayant appris la quantité approximative d’acide sulfurique, il pourra à l’avenir être ajouté à partir d’un cylindre gradué.
L’acide sulfurique doit être ajouté par petites portions afin de ne pas trop acidifier la solution, qui devra ensuite être à nouveau alcalinisée. Chez un travailleur inexpérimenté, l’acidification et l’alcalinisation peuvent se poursuivre indéfiniment. En plus de perdre du temps et des réactifs, une telle régulation déséquilibre la solution nutritive en raison de l’accumulation d’ions inutiles aux plantes.
Alcalinisation de la solution nutritive
Les solutions trop acides sont rendues alcalines avec du sodium caustique (hydroxyde de sodium). Comme son nom l’indique, il est corrosif, il faut donc porter des gants en caoutchouc. Il est recommandé d’acheter de l’hydroxyde de sodium sous forme de pilule. Dans les magasins de produits chimiques ménagers, l’hydroxyde de sodium peut être acheté comme cure-pipe, comme Mole. Dissoudre une pastille dans 0,5 L d’eau et ajouter progressivement la solution alcaline à la solution nutritive en remuant constamment, en vérifiant fréquemment son pH. Aucun calcul mathématique ne peut calculer la quantité d’acide ou d’alcali à ajouter dans un cas donné.
Si vous souhaitez faire pousser plusieurs cultures sur une même palette, vous devez les sélectionner de manière à ce que non seulement leur pH optimal corresponde, mais également les besoins d’autres facteurs de croissance. Par exemple, les jonquilles jaunes et les chrysanthèmes ont besoin d’un pH de 6,8, mais de conditions d’humidité différentes, ils ne peuvent donc pas être cultivés sur la même palette. Si vous donnez aux jonquilles autant d’humidité que les chrysanthèmes, les bulbes de jonquilles pourriront. Dans les expériences, la rhubarbe a atteint son développement maximal à pH 6,5, mais elle pouvait pousser même à pH 3,5. L’avoine, qui préfère un pH d’environ 6, donne de bons rendements à pH 4, si la dose d’azote dans la solution nutritive est fortement augmentée. Les pommes de terre poussent dans une plage de pH assez large, mais elles se développent mieux à un pH de 5,5. En dessous de ce pH, des rendements élevés de tubercules sont également obtenus, mais ils acquièrent un goût aigre. Pour obtenir des rendements de haute qualité maximum, le pH des solutions nutritives doit être ajusté avec précision.